Das cardiovaskuläre System der Vertebraten am Beispiel des Zebrafisches
Die auf dieser Seite behandelten Zebrafischlinien wurden im Rahmen einer Lehrveranstaltung am Max-Planck-Institut für Herz- und Lungenforschung in Bad Nauheim untersucht und dokumentiert. Weitere Informationen zu den genannten Zebrafischlinien und Genen bieten unter anderem die wissenschaftlichen Publikationen Mickoleit et al., 2014 (in Nature Methods) und Kochhan et al., 2013 (in PLoS One).
Zur cardiovaskulären Entwicklung der Vertebraten
Das cardiovaskuläre System setzt sich aus den verschiedenen Blutgefäßen (Arterien, Venen und Kapillaren), dem Blut und dem Herzen zusammen. Seine primäre Funktion besteht darin, Gewebe und Organe mit Sauerstoff und Nährstoffen zu versorgen, aber es trägt auch zur Reinigung bzw. zur Entgiftung des Körpers bei, indem Abfallprodukte oder Toxine zu den Ausscheidungsorganen transportiert werden. Erreicht der Embryo während der Entwicklung eine Größe, bei der eine simple Diffusion zur Verteilung essentieller Substanzen nicht mehr ausreicht, beginnt die Entwicklung des cadiovaskulären Systems, womit es zu den ersten sich entwickelnden Organen in der fortschreitenden Organogenese gehört.
Die einzelnen Strukturen des cardiovaskulären Systems sind mesodermalen Ursprungs, dabei entsteht das Herz aus zwei symmetrischen Strukturen im viszeralen Seitenplattenmesoderm. Im Zuge der Entwicklung wandern die primären Herzfelder zur Mittellinie, bilden eine bilaterale Struktur und fusionieren. Anschließend erfolgt die Morphogenese des primitiven Herzschlauches in das komplexe Gewebe durch Drehung, Faltung, Kammerbildung und Septierung. Mit der Bildung des Herzens beginnt die Entwicklung des vaskulären Systems, welche im Zuge der Embryonalentwicklung eine komplex-verzweigte Struktur entwickelt. Eine anormale Herz- und Vaskulärentwicklung kann zu einer erhöhten Morbidität und Letalität im prenatalen und postnatalen Lebenslauf führen, deren Behandlung mit einem großen Aufwand an chirurgischen Maßnahmen verbunden ist.
Das cardiovaskuläre System am Beispiel des Zebrafisches
Eine korrekt ablaufende Morphogenese des cardiovaskulären Systems und dessen Integritätssicherung ist von entscheidender Bedeutung für die Entwicklung und Gesundheit eines Organismus. Fehlbildungen z.B. in Form von rupturierter Gefäßfehlbildung stellen die Grundlage eines Schlaganfalls dar, welche eine der häufigsten Ursachen für Behinderungen sind. Das Verständnis der Gefäßbildung ist auf Grund seiner Rolle bei verschiedenen Krankheitsbildern Gegenstand intensiver klinischer Untersuchungen. Der Zebrafisch besitzt eine Vielzahl unterschiedlicher Faktoren, die ihn besonders geeignet für Untersuchungen der Gefäßbildung machen. Der Zebrafisch gehört zu den genetisch manipulierbaren Modellorganismen und besitzt zudem aufgrund der Durchsichtigkeit der Embryonen (Abb. 1) eine einfache physikalische Zugänglichkeit, welche ihn für die Untersuchung der Entwicklung des cardiovaskulären Systems besonders interessant macht, da dadurch ein jedes Gefäß und mögliche Fehlentwicklungen in vivo verfolgt werden können.
Im Zebrafisch bedient man sich meist dem Ansatz der forward Genetics, um neue Mutanten zu identifizieren und zu charakterisieren, welche die Entwicklung des cardiovaskulären Systems beeinflussen. Dafür werden transgene Linien erstellt, welche eine Expression eines fluoreszierendes Proteins (GFP) in den Blutgefäßen aufweisen, um anschließend ein umfangreiches
genetisches Screening nach ENU-induzierten Mutanten durchzuführen. Im Praktikum wurden sowohl einfach transgene als auch doppelt transgene Zebrafisch-Linien untersucht. Nachfolgend werden die einzelnen transgenen Linien vorgestellt.
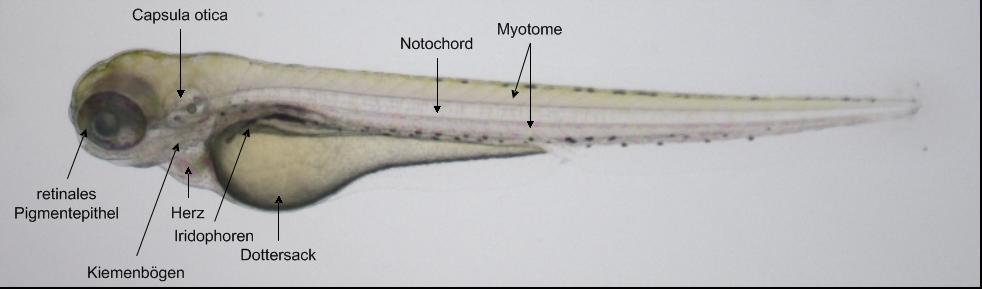 Abb. 1 Laterale Ansicht eines 4 d alten Zebrafischembryos.
Abb. 1 Laterale Ansicht eines 4 d alten Zebrafischembryos.Zebrafischembryonen sind aufgrund ihrer Durchsichtigkeit ein beliebtes Modellsystem zur Untersuchung der Gefäßbildung. Bei einer detaillierten Aufnahme können viele Bultgefäße bereits im Durchlicht beobachtet werden.
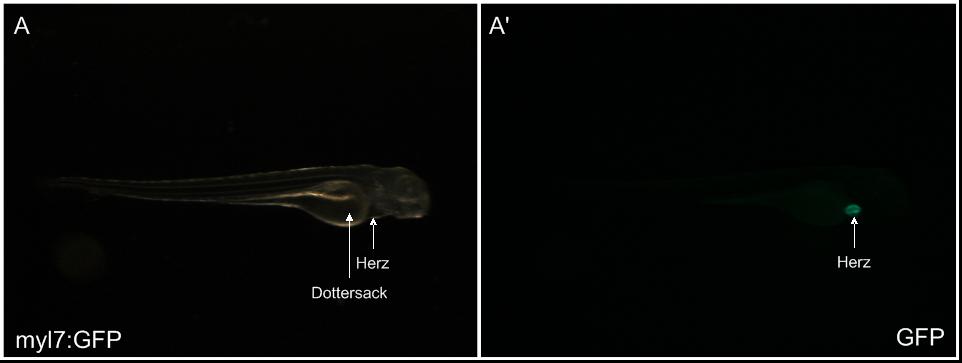
myl7:GFP zeigt eine Expression im Myokard
Das Gen myl7, auch bekannt als cmlc2, codiert für das Cardiac Myosin Light Chain Protein, welchem auch regulatorische Funktionen in der Herzentwicklung zugeschrieben werden. Die einfach transgene Zebrafischlinie myl7:GFP zeigt eine Färbung des Herzens, genauer des Myokards (Abb. 2 A‘). Eine detaillierte Aufnahme (nicht vorhanden) ermöglichte ferner die Unterscheidung des Ventrikels und des Atriums des Herzens.
(Myl7:GFP)(Myl7:nucDS-RED) zeigt ein Signal in Nuclei der Cardiomyozyten
Die doppelt transgene (myl7:GFP)(Myl7:nucDS-RED)-Zebrafischlinie besitzt sowohl ein GFP-Signal als auch ein Signal für dsRED, welche beide an das Protein Myl7 gekoppelt sind. Augenscheinlich unterscheidet sich die Kopplung der Reporterproteine an Myl7, vermutlich was den genauen Bereich der Kopplung der Reporterproteine an Myl7 betrifft, da Unterschiede in der Lokalisation beobachtet werden können. Das GFP-Signal zeigt dabei eine Färbung im Bereich des Myokards (Abb. 3 A“), wobei das Atrium und der Ventrikel hier gut zu unterscheiden sind. Das dsRED-Signal dagegen weist, obwohl eine Lokalisation in den selben Zellen (Cardiomyozyten) zu vermuten ist, da der Marker an dasselbe Protein gekoppelt ist, dennoch eine abweichende, überwiegend nucleäre Lokalisation in den Cardiomyozyten auf (Abb. 3 A‘).
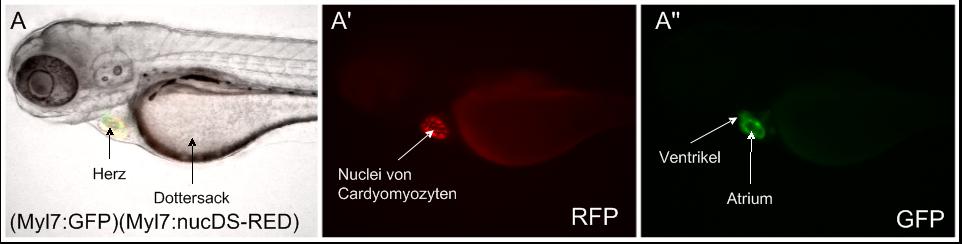 Abb. 3 Expression des eGFP-Konstrukts im Myokard und des dsRED-Konstrukts in Nuclei von Cardiomyozyten der (Myl7:GFP)(Myl7:nucDS-RED)-Zebrafischlinie (laterale Ansicht). Das Signal für dsRED ist in den Nuclei der Cardiomyozyten lokalisiert (A‘). Das GFP-Signal befindet sich im Myokard, wobei hier der Ventrikel und das Atrium gut zu unterscheiden sind (A“).
Abb. 3 Expression des eGFP-Konstrukts im Myokard und des dsRED-Konstrukts in Nuclei von Cardiomyozyten der (Myl7:GFP)(Myl7:nucDS-RED)-Zebrafischlinie (laterale Ansicht). Das Signal für dsRED ist in den Nuclei der Cardiomyozyten lokalisiert (A‘). Das GFP-Signal befindet sich im Myokard, wobei hier der Ventrikel und das Atrium gut zu unterscheiden sind (A“).
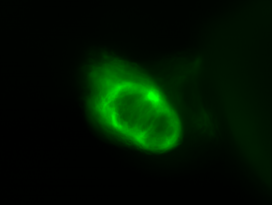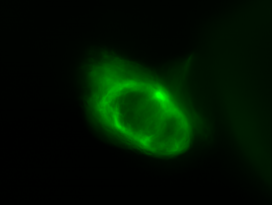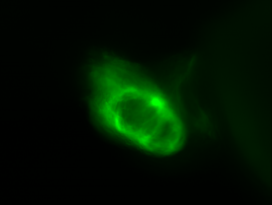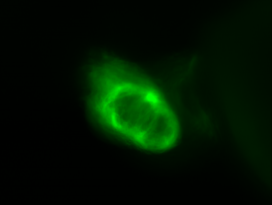 Vid. 1-4 Live-Cell Imaging der (Myl7:GFP)(Myl7:nucDS-RED)-Zebrafischlinie. Roter Kanal zeigt die Lokalisation des ds-RED-Signals in den Nuclei der Cardiomyozyten. Der grüne Kanal zeigt das GFP-Signal in den Cardiomyozyten und damit die Visualisierung des Myokards.
Vid. 1-4 Live-Cell Imaging der (Myl7:GFP)(Myl7:nucDS-RED)-Zebrafischlinie. Roter Kanal zeigt die Lokalisation des ds-RED-Signals in den Nuclei der Cardiomyozyten. Der grüne Kanal zeigt das GFP-Signal in den Cardiomyozyten und damit die Visualisierung des Myokards.fli1:eGFP im Blut und in Zellen der Pharyngealbögen und des Endothels
Die einfach transgene Zebrafischlinie fli1:eGFP weist eine Expression des fluoreszierenden Proteins im Blut und in Zellen des Pharyngealbogens und des Endothels auf. Im anterioren Bereich ist eine starke Expression in den Aortenbögen und im Bereich des zukünftigen Kiefers zu beobachten (Abb. 4 C‘). In einer Vergrößerung des posterioren Bereiches sind die dorsale Aorta, die posteriore Kardinalvene, das dorsale longitudinale anastomotische Gefäß und die intersomitischen Gefäße erkennbar (Abb. 4 C“). Es ist möglich, dass auch weitere Strukturen angefärbt sind, jedoch wäre eine detailliertere Aufnahme notwendig, um dies zu analysieren.
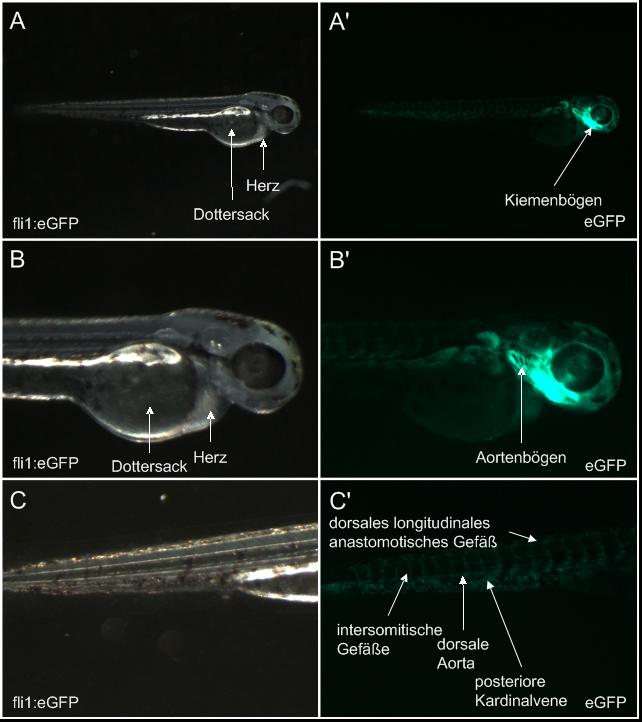 Abb. 4 Expression des eGFP-Konstrukts im vaskulären System der fli1:eGFP
Abb. 4 Expression des eGFP-Konstrukts im vaskulären System der fli1:eGFPZebrafischlinie (laterale Ansicht).
Während ein starkes eGFP-Signal in den Aortenbögen und der Region des zukünftigen Kiefers lokalisiert ist (A‘, B‘), weisen die Strukturen der dorsalen Aorta, der posterioren Kardinalvene, des dorsalen longitudinalen anastomotischen Gefäßes und der intersomitischen Gefäße nur ein moderates Signal von eGFP auf (C‘).
(fli1:eGFP)(HRAS:mCherry) ist membranständig
Die Linie (fli1:eGFP)(HRAS:mCherry) ist eine doppelt transgene Zebrafischlinie, bei der die Expression des eGFP-gekoppelten Fli1-Proteins mit Hilfe des grünen Kanals und die Expression des mCherry-gekoppelten HRAS-Proteins mit Hilfe des roten Kanals dokumentiert werden kann. Das HRAS-Gen, auch bekannt als „v-Ha-ras Harvey rat sarcoma viral oncogene homolog“, codiert für das Protein H-Ras, dessen primäre Funktion in der Regulation der Zellteilung liegt. Dabei leitet das membranständige H-Ras Protein, eine GTPase, für Zellteilung und -wachstum notwendige Signale an den Nucleus weiter.
Wie bereits in der einfach transgenen Zebrafischlinie fli1:eGFP ist das GFP-Signal in den Aortenbögen, im Bereich des zukünftigen Kiefers, in der dorsalen Aorta, der posterioren Kardinalvene, dem dorsalen longitudinalen anastomotischen Gefäß und in den intersomitischen Gefäßen zu beobachten (Abb. 5 A‘, B‘, C‘). Das Signal für das an das H-Ras-Protein gekoppelte mCherry scheint im posterioren Bereich größtenteils in den selben Strukturen lokalisiert zu sein wie das eGFP-Signal in der einfach transgenen Zebrafischlinie fli1:eGFP. Im anterioren Bereich sind jedoch weitere
Strukturen erkennbar, welche in der einfach transgenen Zebrafischlinie fli1:eGFP nicht detektierbar waren. Dazu gehört der primäre Kompfsinus und die Vena cardinalis communis. Auch im Bereich der Kiemenbogenarterien und im Bereich des zukünftigen Kiefers lassen sich Unterschiede zum Signal in der fli1:eGFP-Linie erkennen, da einzelne Gefäße deutlicher von anderen Strukturen abgegrenzt werden können (Abb. 5 B“).
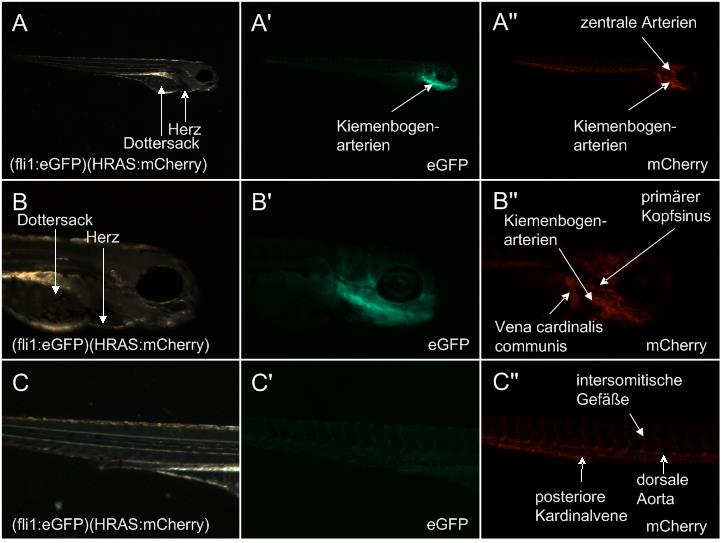 Abb. 5 Expression des eGFP-/mCherry-Konstrukts im vaskulären System der
Abb. 5 Expression des eGFP-/mCherry-Konstrukts im vaskulären System der(fli1:eGFP)(HRAS:mCherry) Zebrafischlinie (laterale Ansicht).
Expressionsmuster des H-Ras-Proteins im posterioren Bereich zeigt Ähnlichkeiten mit dem Expressionsmuster der fli1:eGFP (A‘, B‘, C‘). Im anterioren Bereich sind weitere Strukturen wie der primäre Kopfsinus und die Vena cardinalis communa sowie eine bessere Unterscheidung der Kiemenbogenarterien zu beobachten (B“‘).